नायट्रेट आणि नायट्रेट यांच्यातील फरक
नायट्रेट विरुद्ध नायट्रेट
नायट्रेट आणि नायट्रेट दोन्ही नायट्रोजनचे ऑक्सिअन आहेत. जरी ते दोन्ही सारखे दिसले तरीही त्यांच्यात फरक आहे. हे फरक त्यांच्या संरचना, बंध, भौमितीक आकार, ऑक्सिडेशन स्टेट ऑफ नायट्रोजन, रासायनिक प्रतिक्रिया, त्यांचे वापर आणि इत्यादीच्या बाबतीत असू शकतात. हे फरक प्रामुख्याने येथे दिले आहेत.
NO 3 - आयन हे एचएनओ 3 (नायट्रिक व्ही एसिड) चे संयुग्म्य बेस आहे जे एक मजबूत आम्ल असते. हे नायट्रोजन अणूमध्ये 3 संकरणासह प्लॅनर अणू आहे. सर्व तीन ऑक्सिजनचे अणू समकक्ष आहेत. व्हॅलेन्स गोळ्यामध्ये 24 इलेक्ट्रॉन्स आहेत. नाही 3 - आयनमध्ये 62. 004 जी मोल -1 चे आण्विक वजन आहे. नाही 2 - आयन हे एच एनओ 2 (नायट्रिक III ऍसिड) चे संयुग्मी बेस आहे जे कमकुवत अम्ल (पीकेए = 3.5) आहे. हे
2 संकरण सह एक प्लॅनर रेणू देखील आहे. व्हॅलेन्स शेलमध्ये केवळ 18 इलेक्ट्रॉन आहेत. नाही 2 - आयनमध्ये 46. 006 ग्राम मोल -1 चे आण्विक वजन आहे.
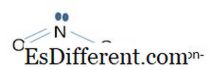

z अण्विक ऑर्बिटल्स यांचा समावेश आहे. येथे, सर्वात कमी ऊर्जेच्या कक्षेत बाँडिंग ऑर्बिटल आहे, मधले एक नॉन-बाँडिंग ऑर्बिटल आहे आणि दुसरा म्हणजे अँटी-बाँडिंग ऑर्बिटल. दोन्ही आयनमध्ये, बाँडिंग ऑर्बिटल्समध्ये σ-bond (सिग्मा-बांड) बनविण्यामध्ये गुंतलेली असते आणि π-bond (pi-bonds) बनविण्यामध्ये नॉन-बाँडिंग ऑर्बिटल्सचा समावेश असतो. म्हणून, NO 3 - आऊट प्रत्येक बॉडमध्ये 1 1 / 3 चे बाँड ऑर्डर आहे. 1 σ-bond पासून आणि 1 / 3 π-बाँडपासून NO मध्ये 2 - आयन, बॉण्ड ऑर्डर 1 1 / 2 आहे. 1 σ-बॉन्ड आणि 1 / 2 π-बाँडस
आयन 120 = 0 आणि 115 0 चे ओएनसीओ बेंज एंगल. नायट्रोजनचे ऑक्सिडेशन स्टेट दोन्हीपैकी 3 - आयन आणि NO 2 - आयन हे अनुक्रमे +5 व +3 आहेत.या कारणांमुळे (विशेषत: बाँडिंगमध्ये फरक), रासायनिक प्रतिक्रिया (जसे की मूलभूतता, ऑक्सिडीझिंग / कमी होण्याची क्षमता, कंपनांच्या थर्मल विघटनयुक्त उत्पादनांमुळे हे आयन बनलेले) देखील वेगळे आहे. सराव मध्ये, 2 - आयन एक कमजोर आधार आहे, तर 3 - आयन एक अतिशय कमजोर आधार आहे. जेव्हा या आयनमध्ये नायट्रोजन अणूचा ऑक्सिडेशन स्टेट विचारात घ्यावयाचा असतो, तेव्हा 2 - आयन हे कमी करणाऱ्या एजंट तसेच ऑक्सिडीझिंग एजंट म्हणून कार्य करू शकते, तसेच 3 - आयन फक्त ऑक्सिडींग एजंट म्हणून कार्य करू शकते. संकेतांसह असलेले कोणतेही आकुंचन - 3 -
आणि 2 - संयुगे असलेले आयन असायला हवेत. जरी ते धातू आकृत्यांमधे कॉम्प्लेक्स बनवतात तेव्हा ते वेगवेगळ्या पद्धतीने वागतात. म्हणजेच, 2 - आयन मोनोडंटेट लिगंड म्हणून काम करते आणि 3 - आयन एक प्रास्ताविक लिगंड म्हणून कार्य करतो. रासायनिक अभिक्रियामध्ये ये फरक आपल्याला त्यांचे उपयोग वेगळं करण्यास मदत करतो. उदाहरणार्थ, नाइट्रेट्सचा वापर सामान्यतः मांस (काही वेळा नायट्रेट्सचा देखील वापर केला जातो) प्रक्रियेत केला जातो आणि नायट्रेट्सचा वापर स्फोटक द्रव्यांच्या निर्मितीसाठी केला जातो. नायट्रेट्स नैसर्गिकरित्या होत आहेत आणि कर्करोगग्रस्त आहेत. पण नायट्रेट्स कर्करोगाच्या नसतात.




